סרטן הוושט
סרטן הוושט הוא גידול ממאיר המתפתח בצינור המעביר מזון מהלוע אל הקיבה. אבחון מדויק והבנת סוג הגידול הם קריטיים לבחירת מסלול הטיפול הנכון. בדף זה נסקור את מאפייני המחלה, דרכי האבחון והשיקולים המקצועיים ב"צומת ההחלטה" – הצעד הראשון בדרך לטיפול מותאם אישית.
מהו סרטן הוושט?
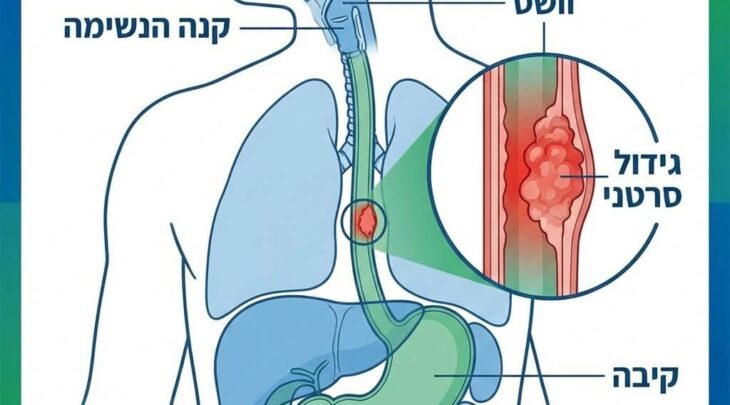
סרטן הוושט (Esophageal Cancer) הוא מחלה שבה תאים ברירית הפנימית של הוושט מתחילים לגדול ולהתחלק ללא בקרה. תאים אלו יוצרים מסה המכונה "גידול ממאיר". הוושט הוא צינור שרירי וחלול, שאורכו בבוגר נע בין 25 ל-30 ס"מ, ותפקידו המרכזי הוא להעביר מזון ונוזלים מהפה אל הקיבה באמצעות תנועה גלית של השרירים.
נקודת התורפה הביולוגית של הוושט
כדי להבין את אופי המחלה, חשוב להכיר מאפיין אנטומי ייחודי של הוושט המהווה "נקודת תורפה" ביולוגית: היעדר שכבת הסרוזה (Serosa). בניגוד לאיברים כמו הקיבה או המעי הגס, העטופים בשכבת הגנה חיצונית קשיחה וחלקה, לוושט אין שכבה כזו. עובדה זו הופכת את דופן הוושט ל"חדירה" יותר עבור תאי הגידול. כתוצאה מכך, הגידול הסרטני עלול לחדור לעומק הדופן ולהתפשט לאיברים חיוניים סמוכים בבית החזה – כמו קנה הנשימה, אבי העורקים והלב – בשלב מוקדם יחסית. בשל כך, ישנה חשיבות עליונה לאבחון מדויק של עומק החדירה כבר בשלבים הראשונים, על מנת לקבוע את אסטרטגיית הטיפול המיטבית.

שכיחות המחלה ונתונים סטטיסטיים
סרטן הוושט נחשב למחלה פחות שכיחה מסרטן המעי הגס, אך היא נמצאת במגמת עלייה בעולם המערבי, במיוחד הסוג הקשור לרפלקס וצרבת כרונית.
- מגדר: שכיחה משמעותית יותר בקרב גברים מאשר בקרב נשים (ביחס של פי 3 עד 4 לטובת הגברים).
- גיל: רוב המקרים מאובחנים מעל גיל 60, אם כי בשנים האחרונות נצפית עלייה באבחון בקרב גילאים צעירים יותר.
- נתונים בישראל: בישראל מאובחנים מדי שנה כמה מאות מקרים חדשים. בעוד שבעבר הסוג הנפוץ היה קשור בעיקר לעישון, כיום אנו רואים עלייה חדה במקרים הנובעים מהשמנת יתר וצרבת ממושכת – נתון המדגיש את חשיבות המעקב בקרב קבוצות סיכון.
סוגי סרטן הוושט: אדנוקרצינומה מול SCC
למרות ששני הסוגים מתפתחים באותו איבר, מדובר בשתי ישויות ביולוגיות שונות לחלוטין. ההבחנה ביניהן קריטית, שכן היא קובעת את מיקום הגידול, את גורמי הסיכון ואת אופי התגובה לטיפולים השונים.
סרטן וושט מסוג אדנוקרצינומה (Adenocarcinoma)
זהו הסוג השכיח ביותר בעולם המערבי כיום, והוא נמצא במגמת עלייה חדה בעשורים האחרונים.
- מיקום: מתפתח בדרך כלל בחלקו התחתון של הוושט, באזור החיבור שבין הוושט לקיבה.
- מקור התאים: הגידול מתפתח מתאי בלוטה (הדומים לתאים המצפים את הקיבה), אשר נוצרים בוושט בעקבות חשיפה ממושכת לחומציות.
- גורמי סיכון עיקריים: השמנת יתר, רפלקס (חזרת תוכן קיבה לוושט) ומצב טרום-סרטני הנקרא "וושט על שם בארט".
סרטן וושט מסוג תאי קשקש (SCC – Squamous Cell Carcinoma)
בעבר זה היה הסוג הנפוץ ביותר, וכיום הוא שכיח פחות במדינות המערב אך עדיין נפוץ מאוד באזורים אחרים בעולם.
- מיקום: יכול להתפתח לכל אורך הוושט, אך לרוב מופיע בחלקו העליון או האמצעי.
- מקור התאים: הגידול מתפתח מהתאים השטוחים והדקים (תאי קשקש) המצפים את החלק הפנימי של הוושט, הדומים במבנם לתאי העור.
- גורמי סיכון עיקריים: עישון כבד וצריכת אלכוהול מוגברת לאורך שנים.
כיצד סוג התא מכתיב את אסטרטגיית הטיפול?
ההבדל הביולוגי בין שני הסוגים מוביל לגישות טיפול שונות. לדוגמה, גידולים מסוג SCC נוטים לעיתים להגיב בצורה דרמטית יותר לטיפולי קרינה וכימותרפיה בהשוואה לאדנוקרצינומה. הבנת סוג התא כבר בשלב הביופסיה מאפשרת לצוות הרפואי להתאים את עוצמת הטיפול ואת סדר הפעולות בצורה המדויקת ביותר למצבכם.
מצרבת כרונית ועד "וושט על שם בארט"
בדומה לסוגי סרטן אחרים במערכת העיכול, סרטן הוושט (במיוחד מסוג אדנוקרצינומה) לרוב אינו מופיע בפתאומיות. מדובר בתהליך הדרגתי הנמשך שנים, שבו תאי הוושט עוברים שינויים מבניים בניסיון להתמודד עם נזקי החומצה העולה מהקיבה.
השלב הראשון: צרבת כרונית ורפלוקס (GERD)
רפלוקס (GERD) הוא מצב שבו השוער שבין הקיבה לוושט אינו נסגר היטב, מה שמאפשר לתוכן חומצי לעלות חזרה אל הוושט. כאשר מצב זה הופך לכרוני (נמשך שנים), החומצה גורמת לדלקת מתמשכת ברירית העדינה של הוושט. עבור רוב האנשים מדובר בטרדה הגורמת לאי-נוחות, אך עבור חלקם, זוהי תחילתה של שרשרת שינויים תאיים.
השלב השני: מהו "וושט על שם בארט" (Barrett’s Esophagus)?
כאשר הוושט נחשף לחומציות גבוהה לאורך זמן, הגוף מנסה "להגן" על עצמו. בתהליך מרתק, הרירית של הוושט מחליפה את התאים המקוריים שלה בתאים עמידים יותר לחומצה, הדומים לאלו המצפים את המעי.
מצב זה נקרא "וושט על שם בארט". אמנם מדובר במנגנון הגנה של הגוף, אך התאים החדשים הללו הם בעלי פוטנציאל להפוך לתאים סרטניים בסיכון גבוה יותר מאשר תאי ושט רגילים.
הסטטיסטיקה המרגיעה: מהם סיכויי המעבר לסרטן הוושט?
כאן חשוב להציג נתון שמרגיע מטופלים רבים: אבחנה של "וושט על שם בארט" אינה אומרת שיש לכם סרטן. למעשה, רוב המטופלים עם "בארט" לעולם לא יפתחו סרטן הוושט.
הסטטיסטיקה הרפואית מראה כי הסיכון למעבר ממצב של "בארט" לסרטן הוושט עומד על כ-0.5% בלבד בשנה. זהו נתון קריטי המלמד כי עם ניהול נכון, ניתן לשלוט במצב בביטחון רב.
כוחה של מניעה: חשיבות המעקב האנדוסקופי
הסיבה שזיהוי "וושט על שם בארט" הוא כה חשוב אינה כדי להפחיד, אלא כדי לאפשר מעקב. מטופלים הנמצאים בתוכנית מעקב מסודרת (Surveillance) עוברים בדיקות גסטרוסקופיה תקופתיות. בבדיקות אלו ניתן לזהות שינויים טרום-סרטניים ראשוניים (דיספלזיה) ולטפל בהם באמצעים פשוטים יחסית, ובכך למנוע את התפתחות הסרטן עוד לפני שהוא נוצר.
תסמינים שחשוב להכיר
בשלבים המוקדמים של סרטן הוושט, לעיתים קרובות אין תסמינים בולטים כלל. ברוב המקרים, הסימנים מופיעים כאשר הגידול גדל ומתחיל להצר את חלל הוושט או להשפיע על הרקמות סביבו. זיהוי מוקדם של סימנים אלו הוא קריטי לפני ההגעה ל"צומת ההחלטה" הטיפולית.
קשיי בליעה (דיספאגיה): "תחושה שהאוכל נתקע"
זהו התסמין הנפוץ ביותר של סרטן הוושט. המטופלים מתארים תחושה של מזון ש"נעצר" או "נתקע" בדרכו למטה, בדרך כלל מאחורי עצם החזה.
- התהליך: לרוב הקושי מתחיל במזונות מוצקים (כמו לחם או בשר). עם הזמן, המטופלים משנים באופן לא מודע את הרגלי האכילה שלהם – לועסים זמן ממושך יותר או עוברים למזונות רכים ונוזליים.
- חשוב לדעת: אם אתם מוצאים את עצמכם מוותרים על מאכלים מסוימים כי הם "קשים מדי לבליעה", יש לפנות לבירור רפואי בהקדם.
ירידה בלתי מוסברת במשקל ושינויים מטבוליים
רבים נוטים לחשוב שהירידה במשקל נובעת רק מהקושי לאכול, אך המציאות הביולוגית מורכבת יותר.
- שינוי מטבולי: הגידול הסרטני משנה את האופן שבו הגוף מנצל אנרגיה. הוא מפריש חומרים הגורמים לפירוק מואץ של רקמות שומן ושריר (מצב הנקרא סרקופניה).
- משמעות: לעיתים הירידה במשקל מקדימה את קשיי הבליעה המשמעותיים. לכן, כל ירידה של מעל 5% ממשקל הגוף תוך חצי שנה ללא דיאטה מכוונת דורשת התייחסות רצינית.
צרבת עמידה וכאב בבית החזה
בעוד שצרבת היא מצב נפוץ, יש לשים לב לשינויים באופיה:
- כאב בזמן בליעה: תחושת צריבה או כאב חד המופיעים ברגע בליעת המזון.
- צרבת שלא מגיבה לטיפול: צרבת שהחמירה פתאום או כזו שאינה משתפרת למרות שימוש בתרופות נוגדות חומצה רגילות.
צרידות ושיעול כרוני
תסמינים אלו עלולים להעיד על כך שהגידול ממוקם בחלק העליון של הוושט ומשפיע על האיברים הסמוכים:
- צרידות: פגיעה או לחץ על העצבים השולטים במיתרי הקול (העצב החוזר).
- שיעול: גירוי של קנה הנשימה או רפלוקס לילי מוגבר כתוצאה מהחסימה בוושט.
חשוב לזכור: תסמינים אלו יכולים להיגרם גם ממצבים רפואיים שפירים אחרים. עם זאת, הופעה של תסמין חדש, ובמיוחד קושי בבליעה, מחייבת בדיקת גסטרוסקופיה או בירור מול רופא/ה מומחה.
אבחון סרטן הוושט וקביעת שלב המחלה
תהליך האבחון נועד לאשר את קיום הגידול ולהעריך במדויק את שלב המחלה (Staging). מידע זה קריטי לבניית תוכנית הטיפול הנכונה עבורכם.
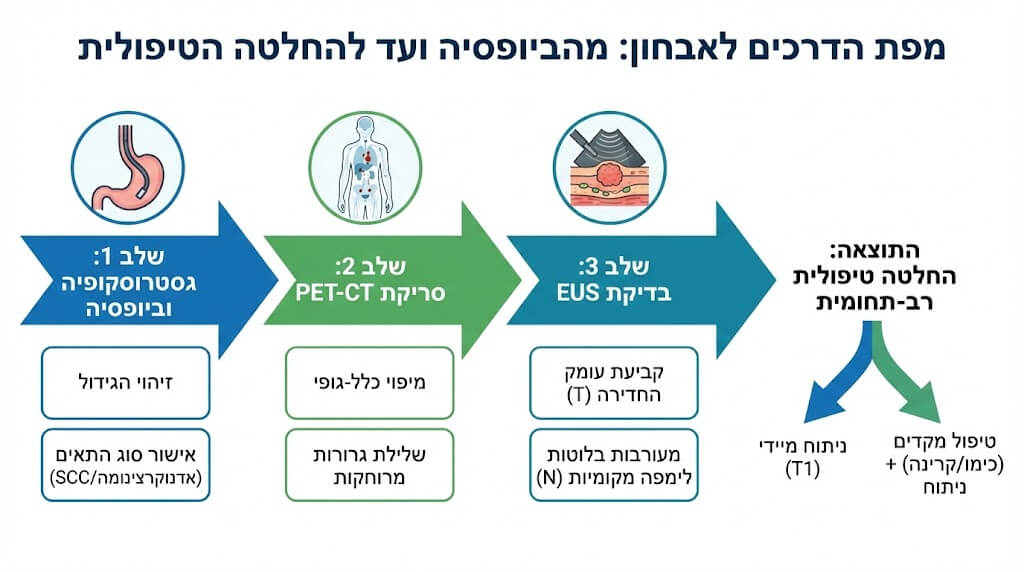
אישור האבחנה – גסטרוסקופיה וביופסיה
הבדיקה הראשונה היא בדרך כלל גסטרוסקופיה, שבה מוחדר צינור דק עם מצלמה אל הוושט.
- ביופסיה: אם מזוהה ממצא חשוד, הרופא/ה יקחו דגימת רקמה קטנה (ביופסיה).
- האבחנה הסופית: הדגימה נבדקת במעבדה פתולוגית, וזו הבדיקה היחידה שמאשרת באופן סופי אם מדובר בגידול סרטני ואת סוג התאים (אדנוקרצינומה או SCC).
בדיקת התפשטות המחלה – CT ו-PET-CT
לאחר אישור האבחנה, יש לבדוק אם הסרטן שלח גרורות לאיברים מרוחקים.
- סריקת CT: מספקת תמונה של החזה, הבטן והאגן כדי לחפש ממצאים חריגים.
- סריקת PET-CT: בדיקה רגישה המזהה פעילות מטבולית של תאי סרטן בכל הגוף. היא חיונית כדי לשלול הימצאות גרורות מרוחקות (שלב M) ולתכנן את היקף הטיפול הקרינתי.
EUS – בדיקת עומק הגידול ובלוטות הלימפה
בדיקה זו, המכונה אולטרסאונד אנדוסקופי, היא הכלי המדויק ביותר להערכת הגידול עצמו וסביבתו הקרובה. בעוד ש-PET-CT בודק את הגוף כולו, ה-EUS מתמקד בגידול עצמו ובסביבתו הקרובה.
- עומק החדירה (שלב T): בעזרת מכשיר אולטרסאונד המורכב על קצה הגסטרוסקופ, המנתח יכול לראות בדיוק בכמה מילימטרים חדר הגידול לתוך דופן הוושט.
- בלוטות לימפה (שלב N): הבדיקה מאפשרת לזהות אם בלוטות לימפה סמוכות נגועות.
- החלטה גורלית: המידע מה-EUS הוא זה שיכריע האם ניתן לגשת לניתוח מיידי או שיש צורך בטיפול מקדים לכיווץ הגידול.
אימונותרפיה וטיפולים ביולוגיים
בעבר, הטיפול האונקולוגי בסרטן הוושט התבסס בעיקר על פרוטוקולים אחידים של כימותרפיה וקרינה. כיום, אנו נמצאים בעידן של רפואה מותאמת אישית, שבה הטיפול נתפר לפי ה"תעודת הזהות" הגנטית של הגידול הסרטני.
ביומרקרים: המפתח להתאמת הטיפול
כדי להחליט על הטיפול המתקדם ביותר, דגימת הגידול שנלקחה בביופסיה עוברת סדרה של בדיקות מעבדה לאיתור סמנים ביולוגיים (Biomarkers). שני הסמנים המרכזיים כיום הם:
- HER2: חלבון שמעודד צמיחה של תאים סרטניים. הוא נמצא בכ-20% מהגידולים מסוג אדנוקרצינומה של הוושט. אם הגידול חיובי ל-HER2, ניתן להוסיף לטיפול תרופות ביולוגיות ממוקדות שחוסמות את החלבון הזה באופן ספציפי.
- PD-L1: זהו חלבון שמשמש את הגידול כדי "להתחבא" ממערכת החיסון. בדיקת רמת הביטוי שלו עוזרת לקבוע האם המטופל יפיק תועלת מטיפול אימונותרפי.
מהי אימונותרפיה ואיך היא עובדת?
בניגוד לכימותרפיה שתוקפת ישירות תאים שמתחלקים מהר, האימונותרפיה אינה תוקפת את הסרטן בעצמה. במקום זאת, היא "מסירה את המסכה" מהגידול ומאפשרת למערכת החיסון הטבעית של המטופל לזהות את תאי הסרטן ולהשמיד אותם.
- היתרון: טיפולים אלו הראו שיפור משמעותי בהישרדות ובאיכות החיים, לעיתים גם במקרים שבהם הכימותרפיה הרגילה פחות השפיעה.
שילוב הכוחות בדרך לריפוי
החידוש הגדול כיום הוא השילוב בין הגישות. לעיתים הטיפול המקדים (לפני הניתוח) יכלול גם אימונותרפיה כדי למקסם את כיווץ הגידול. בשלב גיבוש תוכנית הטיפול האישית, הצוות הרב-תחומי בוחן את הפרופיל הגנטי הזה כדי לוודא שכל הכלים הטיפוליים נרתמים לטובת המטופל ומכינים את הקרקע לניתוח מוצלח.
מבחן הכשירות: להגיע לטיפול בשיא הכוח
ההתמודדות עם סרטן הוושט היא "מרתון" רפואי הדורש מהגוף משאבים רבים. מחקרים מוכיחים כי מצבו הגופני של המטופל ברגע הכניסה לטיפול (בין אם מדובר בכימותרפיה ובין אם בניתוח) הוא אחד המנבאים החזקים ביותר להצלחת התהליך ולמהירות ההתאוששות. מושג זה נקרא Pre-hab (טרום-שיקום).
האתגר המטבולי: שמירה על מסת השריר
כפי שציינו, הגידול הסרטני עלול להפריש חומרים הגורמים לפירוק מואץ של רקמות שומן ושריר (סרקופניה).
- מדוע השריר קריטי? מסת השריר היא "מחסן האנרגיה" של הגוף להתאוששות.
- ההשפעה על הטיפול: מטופלים השומרים על מסת שריר תקינה נוטים לסבול מפחות תופעות לוואי של הכימותרפיה ומחלימים מהר יותר מהניתוח המורכב של כריתת הוושט.
תזונה ככלי טיפולי
בגלל קשיי הבליעה (דיספאגיה), מטופלים רבים מגיעים לאבחנה כשהם כבר במצב של תת-תזונה.
- העשרת קלורית: עוד לפני תחילת הטיפולים, יש צורך בבניית תוכנית תזונתית הכוללת מזונות עתירי חלבון וקלוריות, לעיתים בשילוב תוספי תזונה נוזליים רפואיים.
- ליווי מקצועי: עבודה צמודה עם דיאטנית אונקולוגית היא חלק בלתי נפרד מההכנה לניתוח. המטרה היא לעצור את הירידה במשקל ולחזק את המערכת החיסונית.
פעילות גופנית מותאמת (Pre-habilitation)
למרות התחושה הכללית של עייפות או חולשה, פעילות גופנית מבוקרת היא הכרחית:
- שיפור הרזרבה הנשימתית: ניתוחי וושט מערבים לעיתים קרובות את אזור החזה. חיזוק שרירי הנשימה ושיפור סיבולת לב-ריאה מקטינים משמעותית את הסיכון לסיבוכים ריאתיים לאחר הניתוח.
- שימור הכוח: הליכות יומיות ותרגילי התנגדות קלים עוזרים לגוף להילחם בפירוק השריר המטבולי שהסרטן מנסה להכתיב.
זכרו: כל גרם של שריר וכל קלוריה שנספגת בגוף בשלב זה, הם השקעה ישירה ביכולת שלכם לעבור את הטיפולים בהצלחה ולחזור לשגרה מהר ככל האפשר.
מקום הכירורגיה בטיפול: השאיפה לריפוי מלא
עבור רוב המטופלים המאובחנים עם סרטן הוושט בשלב שטרם שלח גרורות מרוחקות, הניתוח הוא אבן הפינה של הטיפול. בעוד שכימותרפיה וקרינה פועלות לצמצום המחלה, הניתוח הוא הכלי המאפשר את הוצאת הגידול מהגוף ושואף להשגת ריפוי מלא.
הניתוח כטיפול המרכזי להשגת ריפוי
- כריתה של האזור הנגוע בוושט יחד עם בלוטות הלימפה הסמוכות היא הדרך היעילה ביותר לוודא ששולי הגידול נקיים ושלא נותרו תאים סרטניים באזור.
- הצלחת הניתוח נמדדת ביכולת לבצע הסרה מלאה ורדיקלית, תוך שימור מרבי של איכות החיים ושחזור המשכיות מערכת העיכול.
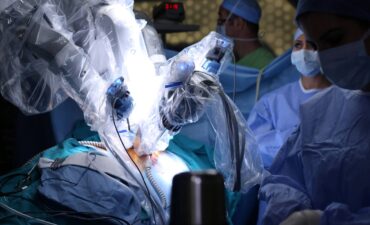
- כיום, רוב הניתוחים מבוצעים בגישות זעיר-פולשניות מתקדמות המאפשרות התאוששות מהירה יותר וחזרה לתפקוד, נושא עליו נרחיב בדף המוקדש לניתוח כריתת הוושט.
צומת ההחלטה: ניתוח מיידי או טיפול מקדים?
לאחר סיום הבירור הרפואי והבנת כלל המדדים, מתקבלת ההחלטה על מסלול הטיפול האופטימלי. בסרטן הוושט, המהירות לגשת לניתוח אינה המדד היחיד להצלחה; לעיתים קרובות, התוצאה הטובה והבטוחה ביותר מושגת דווקא לאחר הכנה מקדימה.
מתי ניגשים לניתוח כצעד ראשון?
ניתוח כצעד ראשון מבוצע לרוב רק במקרים בהם הגידול מתגלה בשלב מוקדם מאוד (שלב T1). במצב זה, הגידול הוא שטחי, לא חדר לשכבות העמוקות של דופן הוושט, ואין כל עדות למעורבות של בלוטות לימפה בבדיקות הדימות.
היתרון שבטיפול המקדים (Neoadjuvant)
ברוב המקרים של סרטן הוושט, הצוות הרפואי ימליץ על שילוב של קרינה וכימותרפיה עוד לפני הניתוח. לגישה זו יש מספר מטרות קריטיות:
- כיווץ הגידול: הקטנת המסה הסרטנית הופכת את הניתוח לבטוח יותר ומאפשרת למנתח להסיר את הגידול במלואו בדיוק רב יותר.
- טיפול בתאים "חבויים": השמדת תאי סרטן מיקרוסקופיים שאולי כבר נפרדו מהגידול הראשוני ונעים בזרם הדם, ובכך הפחתת הסיכון לחזרת המחלה בעתיד.
- מבחן התגובה: האופן שבו הגידול מגיב לטיפול המקדים מעניק לרופאים מידע חשוב על רגישות הגידול לטיפול ועל סיכויי ההחלמה לטווח ארוך.
כיצד מתקבלת ההחלטה?
ההחלטה על מסלול הטיפול אינה מתקבלת על ידי רופא אחד. היא תוצאה של דיון רב-תחומי (Tumor Board) המשלב כירורגים, אונקולוגים, רדיולוגים וגסטרואנטרולוגים. הצוות בוחן יחד את ממצאי ה-EUS וה-PET-CT , את מצבו הגופני של המטופל ואת סוג התא (אדנוקרצינומה או SCC), כדי להתאים לכם את המסלול שיבטיח את סיכויי הריפוי הגבוהים ביותר.
איתור מנתח
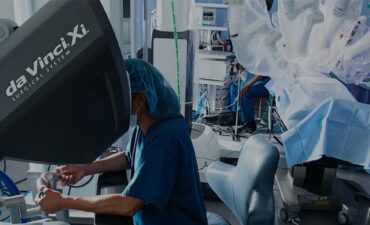
תכירו את הניתוח הרובוטי של דה וינצ'י

מערכת זרועות
הזרועות כוללת מפרקים קטנים, שיודעים לחקות את תנועת כף היד של המנתח ומאפשרות לו טווח תנועה רחב ויכולות לתמרן באזורים צרים ורגישים בדיוק רב. המערכת כוללת מנגנון לביטול הרעד העדין שקיים לנו ביד באופן טבעי.

מערכת ראיית תלת מימד HD D3
הרובוט מצויד מערכת ראיה תלת מימדית מתקדמת, דרכה המנתח רואה את איזור הניתוח בהגדלה וברזולוציה גבוהה, המאפשרים לו לבצע פעולות עדינות ומדויקות.
קונסולת המנתח
הרופא המנתח נמצא לצידך בחדר הניתוח, יושב בקונסולת הניתוח של דה-וינצ', המאפשרת לו שליטה מלאה על מכשור שמשמש לביצוע הניתוח.